
药学院师蕾/叶文才教授团队揭示孤独症“蛋白质合成稳态失衡”共性机制及靶向策略
暨南大学融媒体中心讯 近日,暨南大学生物活性分子与成药性优化全国重点实验室/药学院师蕾研究员和叶文才教授团队在Molecular Psychiatry (Nature子刊,精神病学/神经科学顶刊)在线发表了题为“Correction of eIF4E overactivation rescues translatome imbalance and core ASD-like behaviors in valproic acid-induced offspring mice”的最新研究。师蕾研究员、彭颖慧博士、叶文才教授为论文的共同通讯作者,黄妙奇博士(现中山大学博士后)为论文的第一作者。

文章封面
孤独症谱系障碍(ASD)致病机制复杂,近年研究提示其大脑内mRNA翻译异常与表型相关,但具体的全局变化模式、调控枢纽及因果关系尚不明确。关键难题在于:在ASD高度异质的病因背景下,翻译失调究竟是特定模型的孤立现象,还是不同风险因素汇聚的共性分子事件?目前亟须系统性证据与机制解析。
该研究系统绘制了环境致畸因子丙戊酸(VPA)孕期暴露诱导的孤独症小鼠大脑皮层翻译组图谱,首次阐明了翻译起始因子eIF4E的过度激活是驱动该模型孤独症表型的关键分子枢纽。研究发现,eIF4E的异常活化导致翻译组的不平衡改变,其重要特征是核糖体与线粒体蛋白的过度翻译,进而引发能量代谢紊乱及核心孤独症样行为。更为重要的是,通过跨模型对比分析,团队发现这种“核糖体/线粒体蛋白过度合成”并非VPA模型独有,而是多种遗传与环境风险因素诱导的孤独症模型的共有分子特征。
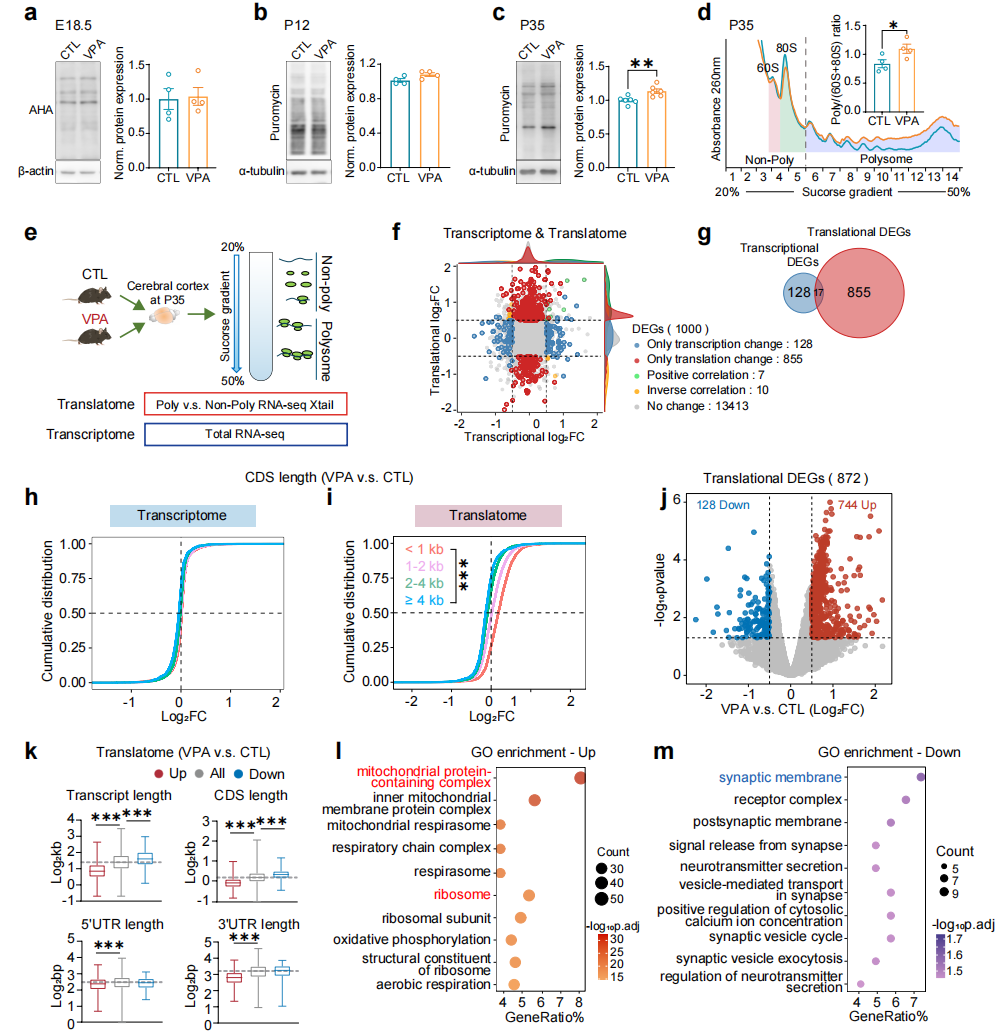
图1.VPA小鼠大脑皮层表现出过度的蛋白质合成和翻译组失衡
在干预策略上,研究取得了突破性进展:在幼年期通过药理学手段纠正eIF4E的异常激活,不仅能有效恢复大脑皮层的蛋白质翻译平衡、下调核糖体及线粒体基因的异常高表达,还能从功能上纠正能量代谢缺陷。令人振奋的是,这种早期干预产生了长期且持久的疗效,显著逆转了模型小鼠的社交障碍与刻板行为等核心症状。这一发现不仅为理解孤独症的复杂病因提供了全新的翻译调控视角,更证实了靶向eIF4E通路作为跨病因治疗策略的巨大潜力,为孤独症临床干预开辟了极具希望的新途径。
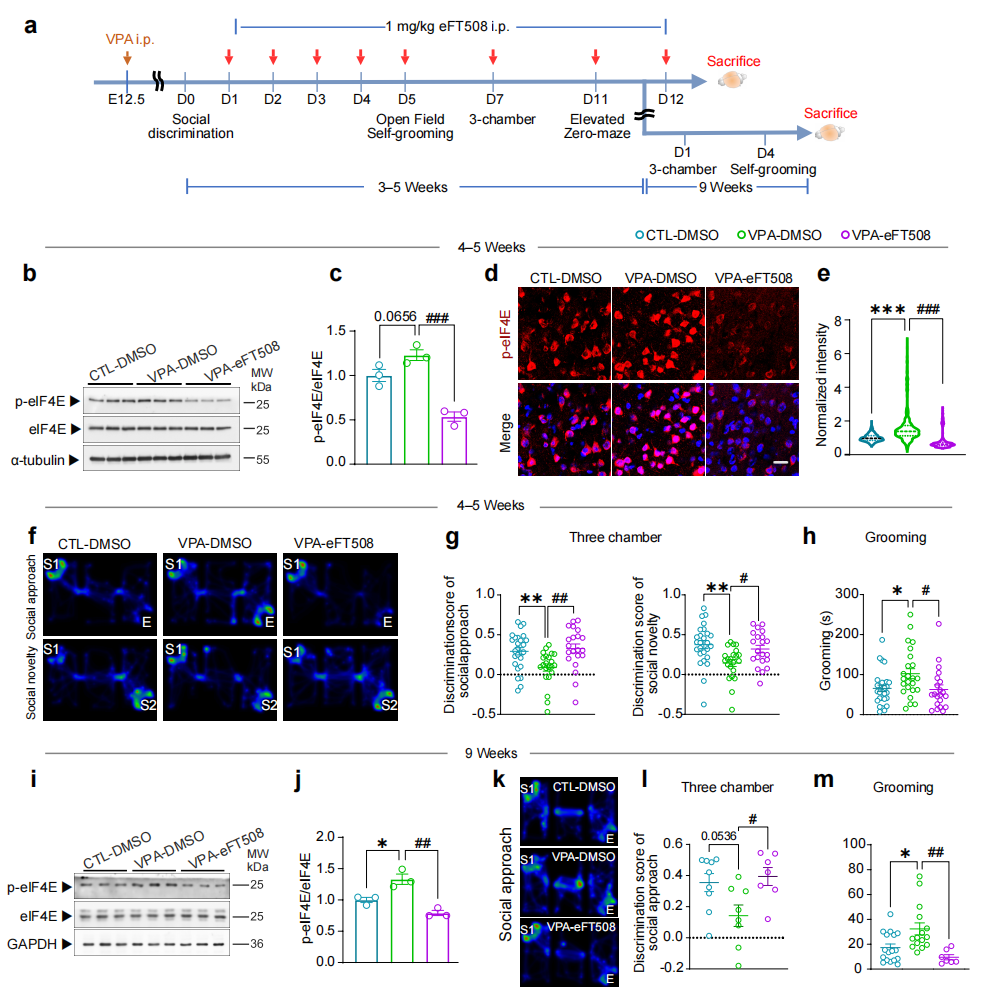
图2.青少年期使用eFT508抑制eIF4E磷酸化,持久改善VPA小鼠孤独症核心行为
该研究得到了国家重点研发计划、国家自然科学基金委、广东省科技厅、暨南大学生物活性分子与成药性优化全国重点实验室的大力支持。
原文链接:https://www.nature.com/articles/s41380-026-03517-3
责编:周会谦




