
粤港澳中枢神经再生研究院吴政、陈功教授团队Acta Pharmaceutica Sinica B:抑制cGAS-STING通路减轻高剂量AAV诱导的神经毒性
暨南大学融媒体中心讯 近日,暨南大学粤港澳中枢神经再生研究院研究团队在药学学报Acta Pharmaceutica Sinica B(IF=14.6)上发表标题为“Attenuating AAV-triggered innate immunity in the adult mouse nervous system via cGAS–STING pathway inhibition”的研究成果。郭耀威博士研究生为该论文的第一作者,粤港澳中枢神经再生研究院雷文亮研究员、陈功教授和吴政研究员为该论文的共同通讯作者。

腺相关病毒(Adeno-associated viruses,AAV)已成为临床基因治疗中的常用载体,AAV的给药剂量与治疗效果之间存在显著的正相关性。然而,临床上AAV基因治疗面临的一个关键挑战是引发不可忽视的炎症和免疫反应,这不仅会削弱治疗效果和持久性,而且在极少数情况下甚至可能危及患者生命。中枢神经系统(CNS)传统上被认为是一个免疫豁免部位,因此AAV基因治疗在CNS中的免疫反应往往被忽视。但是越来越多基础实验特别是大动物模型发现高剂量AAV引起中枢严重免疫反应和神经元丢失。所以,急需有效手段解决在中枢AAV基因治疗中既能使用高剂量AAV递送保证治疗效果,同时又能减轻毒副作用的技术方案。
在对成年小鼠中枢神经系统进行高剂量AAV基因递送时,发现其可强烈激活cGAS-STING先天免疫通路,进而介导显著的神经炎症反应、细胞毒性T细胞浸润及神经元损伤。机制上,AAV衣壳内的DNA基因组是激活该通路的关键,而小胶质细胞作为主要的“哨兵”细胞,通过cGAS感知AAV免疫原性,并产生第二信使cGAMP传递给星形胶质细胞,进而激活STING信号,揭示了两种胶质细胞在介导免疫反应中的协同作用。通过基因敲除(Sting KO小鼠)或药理学抑制(小分子抑制剂H-151)阻断cGAS-STING通路,可显著减轻高剂量AAV引发的神经毒性,同时增强转基因的表达效率,为优化神经基因治疗的安全性及有效性提供了潜在的新策略。这项研究的意义在于在成年小鼠活体水平上阐明了cGAS-STING通路是介导AAV剂量依赖性神经免疫反应的核心机制,并提出了通过靶向该通路来“解耦”治疗性基因递送与有害免疫激活的新理念。这如同为神经基因治疗设计了一个“免疫刹车”系统,而cGAS-STING是该系统的关键枢纽之一。靶向该通路不仅为理解AAV免疫原性提供了全新理论框架,也为临床上安全应用高剂量AAV治疗神经系统疾病开辟了潜在的途径。
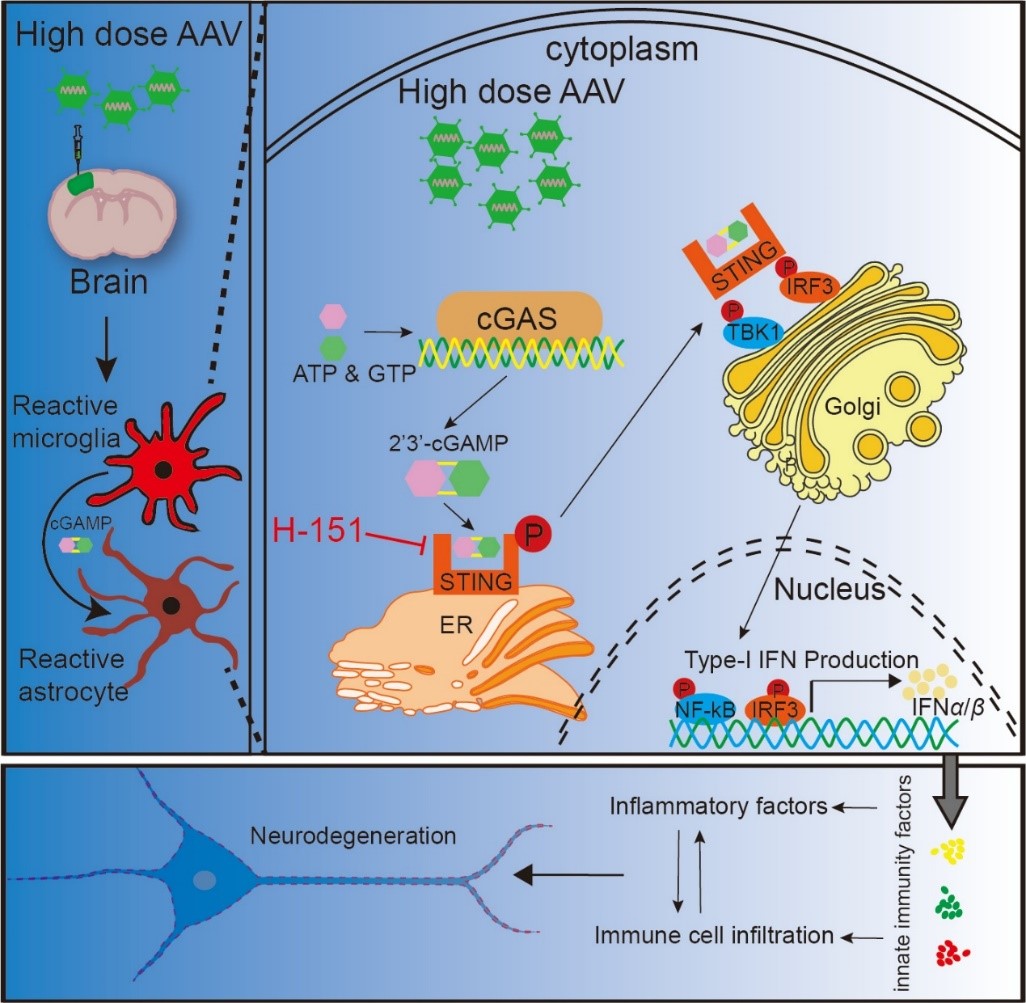
高剂量AAV诱发中枢先天免疫反应的示意图
本项研究受到国家自然科学基金面上和中央高校基本科研业务费专项资金等资助。
原文链接:https://doi.org/10.1016/j.apsb.2026.04.001
责编:常凯丽




